Isovue
La Información De Este Sitio No Constituye Asesoramiento Médico. No Vendemos Nada. No Se Garantiza La Precisión De La Traducción. Descargo De Responsabilidad
Resumen de drogas
¿Qué es isovue-m?
La inyección de isovue-M (iopamidol) es un medio de contraste utilizado para la administración intratecal en neurorradiología, incluida la mielografía (columna total del cuello uterino torácico lumbar) y para la mejora del contraste de la cisternografía tomográfica calculada (CECT) y la ventriculografía.
¿Cuáles son los efectos secundarios de isovue-m?
Isovue
- urticaria
- Dificultad para respirar
- hinchazón de tu cara labios lengua o garganta
- mareos severos
- mareal
- hinchazón
- aumento de peso rápido
- Poco o ningún orinado
- sibilante
- convulsión
- hinchazón in your neck or throat (enlarged thyroid )
- cansancio extremo
- piel seca
- Dolor o rigidez en las articulaciones
- dolor muscular
- debilidad
- ronquera
- aumento de peso
- Mayor sensibilidad a las temperaturas frías
- Dolor o presión del pecho
- dolor que se extiende a tu mandíbula o hombro
- náuseas
- transpiración
- tos repentina
- dificultad para respirar
- tosiendo sangre
- Entumecimiento o debilidad repentina (especialmente en un lado del cuerpo)
- dolor de cabeza severo repentino
- Discurso arrastrado y
- problemas con la visión o el equilibrio
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas enumerados anteriormente.
Los efectos secundarios comunes de isovue-M incluyen:
- dolor de cabeza
- náuseas
- vómitos
- Dolor musculoesquelético (piernas del cuello trasero)
- presión arterial baja (hipotensión)
- dolor y sensación de ardor
- sentirse cálido y
- sofocos .
Busque atención médica o llame al 911 a la vez si tiene los siguientes efectos secundarios graves:
- Síntomas oculares graves, como la pérdida de visión repentina, la visión borrosa de la visión del túnel dolor o hinchazón o ver halos alrededor de las luces;
- Síntomas cardíacos graves como latidos irregulares rápidos o laterales; revoloteando en tu pecho; dificultad para respirar; y mareos repentinos aturdidos o desmayos;
- La confusión de dolor de cabeza severo arrastró el brazo del habla o la debilidad de la pierna, problemas para caminar la pérdida de la coordinación que se siente inestable músculos muy rígidos, fiebre alta sudoración o temblores.
Este documento no contiene todos los efectos secundarios posibles y otros pueden ocurrir. Consulte con su médico para obtener información adicional sobre los efectos secundarios.
Dosis para isovue-m
El rango de dosis de adultos recomendado habitual para Isovue-M es el yodo de 2000-3000 mg.
¿Qué sustancias o suplementos de medicamentos interactúan con isovue-M?
No se deben usar otros productos farmacéuticos o corticosteroides con isovue-M. Se debe tener precaución si ha aumentado la presión intracraneal o la sospecha de absceso tumoral intracraneal o hematoma tener antecedentes de trastorno convulsivo severo enfermedad cardiovascular Alcoholismo crónico de esclerosis múltiple o son ancianos.
Isovue-M durante el embarazo o la lactancia materna
Isovue-M solo debe usarse durante el embarazo si claramente es necesario. Se debe usar precaución si está amamantando.
información adicional
Nuestro centro de medicamentos de efectos secundarios ISovue-M (Iopamidol) proporciona una visión integral de la información de drogas disponible sobre los posibles efectos secundarios al tomar este medicamento.
Información de drogas de la FDA
- Descripción de drogas
- Indicación
- Dosificación
- Efectos secundarios
- Advertencias
- Precauciones
- Sobredosis
- Farmacología clínica
- Guía de medicación
Descripción para isovue-m
Las formulaciones de isovue (inyección de lopamidol) son soluciones estériles acuosas estables y no pirogénicas para la administración intravascular.
Cada ML de isovue-200 (inyección de lopamidol al 41%) proporciona 408 mg de iopamidol con 1 mg de trometamina y 0.26 mg de edetato de calcio disódico. La solución contiene aproximadamente 0.029 mg (0.001 mEq) de sodio y 200 mg de yodo unido orgánicamente por ml.
Cada ML de isovue-250 (inyección de lopamidol 51%) proporciona 510 mg de iopamidol con 1 mg de trometamina y 0. 33 mg de edetato de calcio disodio. La solución contiene aproximadamente 0.036 mg (0.002 mEq) de sodio y 250 mg de yodo unido orgánicamente por ml.
Cada ml de isovue-300 (inyección de lopamidol 61%) proporciona 612 mg de iopamidol con 1 mg de trometamina y 0.39 mg de edetato de calcio disodio. La solución contiene aproximadamente 0.043 mg (0.002 mEq) de sodio y 300 mg de yodo unido orgánicamente por ml.
Cada ml de isovue-370 (inyección de lopamidol 76%) proporciona 755 mg de iopamidol con 1 mg de trometamina y 0.48 mg de edetato de calcio disodio. La solución contiene aproximadamente 0.053 mg (0.002 mEq) de sodio y 370 mg de yodo unido orgánicamente por ml.
El pH de los medios de contraste isovue se ha ajustado a 6.5-7.5 con ácido clorhídrico y/o hidróxido de sodio. Los datos fisicoquímicos pertinentes se observan a continuación. Isovue (inyección de lopamidol) es hipertónico en comparación con el líquido plasmático y cefalorraquídeo (aproximadamente 285 y 301 mOSM/kg de agua respectivamente).
| Iopamidol | ||||
| Parámetro | 41% | 51% | 61% | 76% |
| Concentración (MGL/ML) | 200 | 250 | 300 | 370 |
| Osmolalidad @ 37 ° C (agua MOSM/kg) | 413 | 524 | 616 | 796 |
| Viscosidad (CP) @ 37 ° C | 2.0 | 3.0 | 4.7 | 9.4 |
| @ 20 ° C | 3.3 | 5.1 | 8.8 | 20.9 |
| Gravedad específica a 37 ° C | 1.227 | 1.281 | 1.339 | 1.405 |
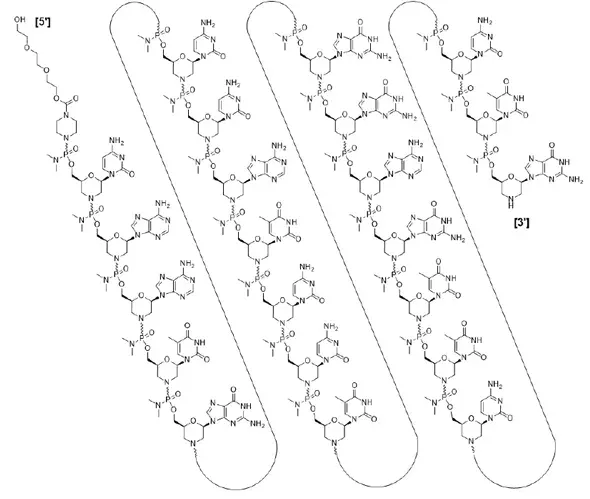
El lopamidol se designa químicamente como (S) -nn'-bis [2-hidroxi-1- (hidroximetil) -etil] 246-triiodo-5-lactamidoisoisoftalamida. Fórmula estructural:
 |
Usos para isovue-m
La isovue (inyección de iopamidol) está indicada para la angiografía en todo el sistema cardiovascular en adultos, incluida la arteriografía coronaria cerebral y periférica, la arteriografía coronaria y la venografía visceral selectiva de la aortografía (flebografía) y en pacientes pediátricos para angiocardiografía; o para el uso intravenoso en imágenes de la cabeza y el cuerpo para adultos y pediátricos para la cabeza y el cuerpo de la cabeza y el cuerpo (ver más abajo).
Imágenes de cabeza de CT
La isovue puede usarse para refinar la precisión de diagnóstico en áreas del cerebro que de otro modo no se han visualizado satisfactoriamente.
Tumor
Isovue puede ser útil para investigar la presencia y el alcance de ciertas neoplasias tales como: gliomas incluidos gliomas malignos glioblastomas astrocytomas oligodendrogliomas y gangliomas ependymomas meduloblastomas Meningiomas neuromas neuromas pituitomas adenomas Craniopharyngiomás germanales y metales y metales y metenomas y metanminomas y metenales. No se ha demostrado la utilidad de la mejora del contraste para la investigación del espacio retrobulbar y en casos de bajo grado o glioma infiltrativo.
En las lesiones calcificadas hay menos probabilidad de mejora. Después de la terapia, los tumores pueden mostrar una mejora disminuida o sin.
La opacificación del Vermis inferior después de la administración de medios de contraste ha resultado en un diagnóstico falso positivo en varios estudios normales.
Condiciones no neoplásicas
Isovue puede ser beneficioso en la mejora de la imagen de lesiones no neoplásicas. Las infartos cerebrales del inicio reciente pueden visualizarse mejor con la mejora del contraste, mientras que algunos infartos se oscurecen si se utilizan medios de contraste. El uso de medios de contraste yodados da como resultado una mejora del contraste en aproximadamente el 60 por ciento de las infartos cerebrales estudiadas de una a cuatro semanas desde el inicio de los síntomas.
Los sitios de infección activa también pueden mejorarse después de la administración de medios de contraste. Las malformaciones y aneurismas arteriovenosos mostrarán una mejora de contraste. Para estas lesiones vasculares, la mejora probablemente depende del contenido de yodo del grupo de sangre circulante.
Los hematomas y los sangrantes intraparenquimatales rara vez demuestran una mejora de contraste. Sin embargo, en casos de coágulo intraparenquimatoso para el cual no existe una explicación clínica obvia, la administración de medios de contraste puede ser útil para descartar la posibilidad de malformación arteriovenosa asociada.
Imágenes del cuerpo de CT
La isovue (inyección de iopamidol) puede usarse para mejorar la isovue tomográfica calculada (inyección de iopamidol) para mejorar las imágenes tomográficas calculadas para la detección y evaluación de lesiones en el hígado de páncreas aorta aorta mediastinum cavidad abdominal cavidad abdominal y espacio retroperitoneal.
La mejora de la tomografía computarizada con isovue puede ser beneficioso para establecer diagnósticos de ciertas lesiones en estos sitios con mayor seguridad de la que es posible con la TC solo y en el suministro de características adicionales de las lesiones (por ejemplo, delineación hepática de absceso antes del drenaje percutáneo). En otros casos, el agente de contraste puede permitir la visualización de lesiones que no se ve con la TC sola (por ejemplo, extensión tumoral) o puede ayudar a definir lesiones sospechosas observadas con TC no mejorada (por ejemplo, quiste pancreático).
La mejora del contraste parece ser mayor dentro de los 60 a 90 segundos después de la administración de bolo del agente de contraste. Por lo tanto, la utilización de una técnica de escaneo continuo (tomografía computarizada dinámica) puede mejorar la mejora y la evaluación diagnóstica del tumor y otras lesiones, como un absceso ocasionalmente que revela una enfermedad insospechada o más extensa. Por ejemplo, un quiste puede distinguirse de una lesión sólida vascularizada cuando se comparan precontraste y escaneos mejorados; La masa no perfundida muestra la absorción de rayos X sin cambios (número de TC). Una lesión vascularizada se caracteriza por un aumento en el número de TC en los pocos minutos después de un bolo de agente de contraste intravascular; Puede ser un tejido benigno o normal maligno, pero probablemente no sería un hematoma de quiste u otra lesión no vascular.
Debido a que el escaneo no mejorado puede proporcionar información de diagnóstico adecuada en el paciente individual, la decisión de emplear la mejora del contraste que puede estar asociada con el riesgo y una mayor exposición a la radiación debe basarse en una evaluación cuidadosa de otros hallazgos de TC radiológicos y desinteresados clínicos.
Dosis para isovue-m
General
Los productos farmacéuticos parenterales deben ser inspeccionados visualmente para partículas y decoloración antes de la administración siempre que la solución y el contenedor lo permitan. Las soluciones de iopamidol deben usarse solo si son claras y dentro del rango de color amarillo pálido normal y dentro del color amarillo normal. Deseche cualquier producto que muestre signos de cristalización o daño al sistema de cierre del contenedor que incluye el tapón del recipiente de vidrio y/o el engarzado.
Es deseable que las soluciones de agentes de diagnóstico radiopaco para uso intravascular sean a temperatura corporal cuando se inyectan. Las técnicas estériles deben usarse con cualquier inyección intravascular.
La transferencia de isovue desde el contenedor de paquetes a granel de Isovue Imaging debe realizarse utilizando técnica aséptica. El cierre del paquete a granel de imágenes puede ser penetrado solo una vez con un componente estéril adecuado del sistema de gestión de contraste de contraste de inyección de contraste automatizado o un conjunto de transferencia de medios de contraste aprobado o despejado para su uso con este paquete a granel de imágenes.
Los pacientes deben estar bien hidratados antes y después de la administración de isovue (inyección de iopamidol).
Al igual que con todos los agentes de contraste radiopaco, solo se debe utilizar la dosis más baja de isovue necesaria para obtener una visualización adecuada. Una dosis más baja reduce la posibilidad de una reacción adversa. La mayoría de los procedimientos no requieren el uso de una dosis máxima o la mayor concentración disponible de isovue; La combinación de la concentración de dosis e isovue que se utilizará debe ser cuidadosamente individualizada y factores como el tamaño del tamaño del cuerpo de la edad del vaso y su tasa de flujo sanguíneo, se debe considerar la patología y el grado y el grado de las estructuras o el área requeridas por la opacificación.
Arteriografía cerebral
Se deben usar isovue-300 (inyección de iopamidol 300 mg de yodo/ml). La inyección individual habitual por punción carótida o cateterismo transfemoral es de 8 a 12 ml con dosis múltiples totales de hasta 90 ml.
Arteriografía periférica
Isovue-300 generalmente proporciona una visualización adecuada. Para la inyección en la arteria femoral o la arteria subclavia de 5 a 40 ml se pueden usar; Para la inyección en la aorta para una escorrentía distal de 25 a 50 ml se puede usar. Se han administrado dosis de hasta un total de 250 ml de isovue-300 durante la arteriografía periférica.
Venografía periférica (flebografía)
ISovue-300 debe usarse. La dosis habitual es de 15 ml a 100 ml por extremidad inferior.
¿Cuántas horas entre las dosis de Buspar
La dosis total combinada para inyecciones múltiples no debe exceder los 230 ml.
Arteriografía visceral selectiva y aortografía
Se debe usar isovue-370 (inyección de iopamidol 370 mg de yodo/ml). Se pueden requerir dosis de hasta 50 ml para la inyección en los vasos más grandes, como la aorta o la arteria celíaca; Se pueden requerir dosis de hasta 10 ml para la inyección en las arterias renales. A menudo, las dosis más bajas serán suficientes. La dosis total combinada para inyecciones múltiples no ha excedido 225 ml.
Angiocardiografía pediátrica
Isovue-370 debe usarse. La angiocardiografía pediátrica se puede realizar mediante inyección en una gran vena periférica o ser caracterización directa del corazón. El rango de dosis habitual para inyecciones individuales se proporciona en la siguiente tabla:
| Inyección única | Rango de dosis habitual |
| Edad | ml |
| <2 years | 10-15 |
| 2–9 años | 15-30 |
| 10-18 años | 20-50 |
La dosis recomendada habitual para inyecciones acumulativas se proporciona en la siguiente tabla.
| Inyección acumulativa | Dosis habitual recomendada |
| Edad | ml |
| <2 years | 40 |
| 2–4 años | 50 |
| 5–9 años | 100 |
| 10-18 años | 125 |
Arteriografía coronaria y ventriculografía
Isovue-370 debe usarse. La dosis habitual para las inyecciones selectivas de la arteria coronaria es de 2 a 10 ml. La dosis habitual para la ventriculografía o para la opacificación no selectiva de múltiples arterias coronarias después de la inyección en la raíz aórtica es de 25 a 50 ml. La dosis total para los procedimientos combinados no ha excedido los 200 ml. El monitoreo de EKG es esencial.
Tomografía computarizada
CT de la cabeza
La dosis sugerida para Isovue-300 es de 100 a 200 ml por administración intravenosa. Las imágenes se pueden realizar inmediatamente después de completar la administración.
CT del cuerpo
El rango de dosis de adultos habitual para Isovue-300 es de 100 a 200 ml administrado por una rápida infusión intravenosa o inyección de bolo.
También se pueden utilizar dosis equivalentes de Isovue-370 basadas en el contenido de yodo unido orgánicamente.
La dosis total para el procedimiento de CT no debe exceder los 60 gramos de yodo.
Tomografía computarizada pediátrica
La dosis recomendada para su uso en niños para la tomografía computarizada mejorada de contraste es de 1.0 ml/kg a 3.0 ml/kg para isovue-300. No debe ser necesario exceder una dosis total de 30 gramos de yodo.
Incompatibilidades de drogas
Muchos agentes de contraste radiopaco son incompatibles in vitro con algunos antihistamínicos y muchas otras drogas; Por lo tanto, ningún otro producto farmacéutico debe mezclarse con agentes de contraste.
Manejo de drogas
Los productos farmacéuticos parenterales deben ser inspeccionados visualmente para partículas y decoloración antes de la administración siempre que la solución y el contenedor lo permitan. Las soluciones de iopamidol deben usarse solo si son claras y dentro del rango de color amarillo pálido normal y dentro del color amarillo normal. Deseche cualquier producto que muestre signos de cristalización o daño al sistema de cierre del contenedor que incluye el tapón del recipiente de vidrio y/o el engarzado.
Instrucciones para el uso adecuado del paquete a granel de Isovue Imaging
El paquete a granel de Isovue Imaging se utiliza para dispensar múltiples dosis individuales de inyección de iopamidol para múltiples pacientes que utilizan un sistema de gestión de contraste de inyección de contraste automatizado o un conjunto de transferencia de medios de contraste aprobado o borrado para su uso con este agente de contraste en este paquete a granel de imágenes. Las preparaciones de inyección de cloruro de sodio al 0,9% USP con un puerto estéril para un conjunto de administración intravenosa se utilizarán con el paquete a granel de Isovue Imaging y los sistemas de inyección de contraste automatizados o los sistemas de gestión de contraste de contraste aprobados para su uso con el paquete a granel de IsoVue Imaging. Consulte el etiquetado de medicamentos y dispositivos para obtener información sobre dispositivos indicados para su uso con este paquete y técnicas a granel de imágenes para ayudar a garantizar un uso seguro.
- El paquete a granel de Isovue Imaging se utilizará solo en una habitación designada para procedimientos radiológicos que involucren la administración intravascular de un agente de contraste.
- La transferencia de isovue desde el paquete a granel de imágenes debe realizarse utilizando técnica aséptica. Antes de penetrar en el cierre del contenedor, la cara del tapón del contenedor con 70% de alcohol isopropílico. El cierre del contenedor puede ser penetrado solo una vez con un componente estéril adecuado del sistema de gestión de contraste de inyección de contraste automatizado o un conjunto de transferencia de medios de contraste aprobado o despejado para su uso con este paquete a granel de imágenes.
- Una vez que el paquete a granel de imágenes está perforado, no debe retirarse del área de trabajo durante todo el período de uso y la botella debe mantenerse en una posición invertida de modo que el contenido del contenedor esté en contacto continuo con el conjunto de dispensaciones.
- Se permite que un tiempo de uso máximo de 10 horas desde la entrada de cierre inicial complete la transferencia de fluidos. Cualquier inyección de isovue no utilizada debe ser descartada 10 horas después de la punción inicial del paquete a granel de imágenes.
- Después del cierre del contenedor, se perfora si la integridad del paquete a granel de imágenes y el sistema de entrega no pueden estar asegurados, aunque se debe descartar la supervisión continua directa, se debe descartar el paquete a granel de imágenes y todos los desechables asociados para el sistema de gestión de contraste de inyección de contraste automatizado o el conjunto de transferencia de medios de contraste.
- La temperatura de almacenamiento del recipiente de paquete a granel de Isovue Imaging después de que se haya ingresado el cierre no debe exceder los 25 ° C (77 ° F); Sin embargo, es deseable que el contenido se calienta a la temperatura corporal antes de la inyección.
- Si se usa la inyección de cloruro de sodio al 0,9%, USP se utilice, prepare el puerto intravenoso de acuerdo con la sección de dosificación y administración de la información de prescripción aprobada del producto.
- Uso de dosis múltiple de inyección de cloruro de sodio al 0,9% USP:
- La inyección de cloruro de sodio al 0,9% USP solo debe usarse para administrar múltiples dosis a múltiples pacientes cuando se usa con un sistema de inyección de contraste automatizado o un sistema de manejo de contraste aprobado o eliminado para el uso de dosis múltiple de inyección de cloruro de sodio al 0,9%.
- El puerto de administración intravenoso del contenedor de cloruro de sodio puede ser penetrado solo una vez con un componente estéril adecuado del sistema de gestión de contraste aprobado para su uso con el paquete a granel de Isovue Imaging utilizando una técnica aséptica. Se permite que un tiempo de uso máximo de 10 horas desde la entrada de cierre inicial complete la transferencia de fluido. Cualquier cloruro de sodio no utilizado debe descartarse 10 horas después de la punción inicial del contenedor de inyección de cloruro de sodio al 0,9%. El contenedor de inyección de cloruro de sodio al 0,9% USP se utilizará solo en un área designada para procedimientos radiológicos que involucran la administración intravascular de contraste. Todas las instrucciones anteriores en c. a través de e. Para el paquete a granel de Isovue Imaging se debe seguir para el contenedor de inyección de cloruro de sodio al 0,9%. Corre la etiqueta salina proporcionada con el paquete a granel Isovue Imaging en el contenedor de inyección de cloruro de sodio al 0,9%.
- Uso de dosis única de inyección de cloruro de sodio al 0.9% USP: Uso de acuerdo con la información de prescripción de los fabricantes.
Que suministrado
Almacenamiento y manejo
Isovue-300 (inyección de iopamidol 61%)
Diez paquetes a granel de 200 ml de imágenes ( NDC 0270-1315-45)
Seis paquetes a granel de 500 ml de imágenes ( NDC 0270-1315-95)
Isovue-370 (inyección de iopamidol 76%)
Diez paquetes a granel de 200 ml de imágenes ( NDC 0270-1316-45)
Seis paquetes a granel de 500 ml de imágenes ( NDC 0270-1316-95)
Almacenamiento
Almacene a 20-25 ° C (68-77 ° F). [Ver USP]. Proteger de la luz.
Isovue es una marca registrada de Bracco Diagnostics Inc.
Fabricado por: Bipso GMBH 78224 Singen (Alemania). Revisado: abril de 2023
¿Para qué se usa Opana er
Efectos secundarios para isovue-M
Las reacciones adversas después del uso de iopamidol suelen ser autodilimitadas y transitorias leves a moderadas.
En la angiocardiografía (597 pacientes), las reacciones adversas con una incidencia estimada del uno por ciento o superior son: sofocos 3.4%; angina pectoris 3.0%; Flushing 1.8%; bradicardia 1.3%; hipotensión 1.0%; colmenas 1.0%.
En un ensayo clínico con 76 pacientes pediátricos sometidos a angiocardiografía 2 reacciones adversas (2.6%), se informaron de forma remota a los medios de contraste. Ambos pacientes tenían menos de 2 años de edad tenían enfermedad cardíaca cianótica con anormalidades ventriculares derechas subyacentes y circulación pulmonar anormal. En un paciente, la cianosis preexistente se intensificó transitoriamente después de la administración de medios de contraste. En el segundo paciente, la disminución de la perfusión periférica preexistente se intensificó durante 24 horas después del examen. (Ver PRECAUCIONES Sección para información sobre la naturaleza de alto riesgo de estos pacientes).
La inyección intravascular de los medios de contraste se asocia frecuentemente con la sensación de calor y dolor, especialmente en la arteriografía periférica y la venografía; El dolor y el calor son menos frecuentes y menos severos con isovue (inyección de iopamidol) que con la inyección de diatrizoato de meglumina y diatrizoato de sodio.
La siguiente tabla de incidencia de reacciones se basa en estudios clínicos con isovue en aproximadamente 2246 pacientes.
| Reacciones adversas | ||
| Sistema | > 1% | Incidencia general estimada ≤ 1% |
| Cardiovascular | ninguno | taquicardia hipotensión hipertensión isquemia miocárdica colapso circulatorio Depresión del segmento S-T bigemines extrasistoles fibrilación ventricular Angina de cofre bradicardia ataque isquémico transitorio tromboflebitis |
| Nervioso | Dolor (2.8%) sensación de ardor (1.4%) | reacción vasovagal hormigueo en los brazos mueca debilidad |
| Digestivo | náuseas (1.2%) | vómitos anorexia |
| Respiratorio | ninguno | constricción de garganta dyspnea edema pulmonar |
| Piel y apéndices | ninguno | erupción urticaria prurito rubor |
| Cuerpo en su conjunto | sofocos (1.5%) | dolor de cabeza fiebre escalofríos sudoración excesiva espasmo trasero |
| Sentidos especiales | Calidez (1.1%) | Alteraciones del sabor congestión nasal perturbaciones visuales |
| Urogenital | ninguno | retención urinaria |
Independientemente del agente de contraste empleado, la incidencia general estimada de reacciones adversas graves es mayor con arteriografía coronaria que con otros procedimientos. Descompensación cardíaca arritmias graves o isquemia o infarto de miocardio se han informado con isovue y pueden ocurrir durante arteriografía coronariay left ventriculography .
Después de las inyecciones coronarias y ventriculares, ciertos cambios electrocardiográficos (aumento de QTC aumentó la amplitud de la onda t R-R) y ciertos cambios hemodinámicos (presión sistólica disminuida) ocurrieron con menos frecuencia con isovue (inyección de iopamidol) que con la inyección de diatrizoato de meglumina y diatrizoato de sodio; El aumento de LVEDP ocurrió con menos frecuencia después de las inyecciones de iopamidol ventricular.
En aortografía Los riesgos de los procedimientos también incluyen lesiones en la aorta y los órganos vecinos de punción pleural daños renales, incluido el infarto y la necrosis tabular aguda con oliguria y anuria, el llenado selectivo accidental de la arteria renal renal durante el procedimiento de translumbar en la presencia de la enfermedad de la enfermedad síndica pre-existir de la enfermedad síndica de la enfermedad síndica de la enfermedad síndica de la enfermedad síndica con el asociación síndica síndica de la enfermedad síndica con el estado de la enfermedad síndica de la ruta síndica con el asociación síndica síndica de la ruta de la ruta de la ruta de la ruta. mielitis.
Se han informado las siguientes reacciones adversas para iopamidol:
Cardiovascular: arritmia espasmos arteriales enjuagando el dolor del pecho de vasodilatación parto cardiopulmonar;
Nervioso Sistema: confusión parestesia mareos temporal ceguera cortical temporal amnesia convulsiones parálisis coma;
Respiratorio: Aumento de la tos estornudante de asma apnea el edema laríngeo rhinitis tórax rinitis;
Piel y apéndices: Dolor en el sitio de inyección generalmente debido a la extravasación y/o al edema de edema de edema periorbital de hinchazón eritemática;
Urogenital: dolor hematuria;
Sentidos especiales: Conjuntivitis de lacrimación con picazón acuosa de la lacrimación;
Musculoesquelético: espasmo muscular movimiento de pierna involuntaria;
Cuerpo en su conjunto: Temblores Reacción anafilactoides malestar (caracterizado por síntomas respiratorios cardiovasculares y cutáneos);
Digestivo: Retching severo y calambres abdominales asfixiados. Algunos de estos pueden ocurrir como consecuencia del procedimiento. También pueden ocurrir otras reacciones con el uso de cualquier agente de contraste como consecuencia del peligro de procedimiento;
Estos incluyen hemorragia o pseudoaneurismas en el sitio de punción parálisis del plexo braquial después de las inyecciones de la arteria axilar del dolor torácico del dolor en el pecho y los cambios transitorios en las pruebas de química hepateral. Trombosis arterial El desplazamiento de las placas arteriales trombosis venosa La disección de los vasos coronarios y la detención sinusal transitoria son complicaciones raras.
General Reacciones adversas To Contrast Media
Las reacciones que se sabe que ocurren con la administración parenteral de agentes de contraste iónico yodado (ver el listado a continuación) son posibles con cualquier agente no iónico. Aproximadamente el 95 por ciento de las reacciones adversas que acompañan al uso de otros agentes de contraste administrados por vía intravascularmente soluble en agua son de grado de leve a moderado en grado. Sin embargo, se han producido reacciones y muertes que amenazan la vida principalmente de origen cardiovascular. Informar incidentes de muerte por la administración de otros medios de contraste yodados varían de 6.6 por 1 millón (0.00066 por ciento) a 1 en 10000 pacientes (0.01 por ciento). La mayoría de las muertes ocurren durante la inyección o de 5 a 10 minutos después, la característica principal es un paro cardíaco con enfermedad cardiovascular como el principal factor agravante. Los informes aislados de colapso y shock hipotensos se encuentran en la literatura. La incidencia de shock se estima en 1 de 20000 (0.005 por ciento) pacientes.
Las reacciones adversas a los medios de contraste inyectables se dividen en dos categorías: reacciones quimiotóxicas y reacciones idiosincráticas. Las reacciones quimiotóxicas resultan de las propiedades fisicoquímicas del medio de contraste, la dosis y la velocidad de inyección. En esta categoría se incluyen todas las perturbaciones y lesiones hemodinámicas a los órganos o vasos perfundidos por el medio de contraste. Las reacciones idiosincráticas incluyen todas las demás reacciones. Ocurren con más frecuencia en pacientes de 20 a 40 años. Las reacciones idiosincráticas pueden o no depender de la cantidad de fármaco inyectado la velocidad de inyección el modo de inyección y el procedimiento radiográfico. Las reacciones idiosincráticas se subdividen en menores intermedios y graves. Las reacciones menores son autolimitadas y de corta duración; Las reacciones severas son potencialmente mortales y el tratamiento es urgente y obligatorio.
La incidencia informada de reacciones adversas a los medios de contraste en pacientes con antecedentes de alergia es el doble de la población general. Los pacientes con antecedentes de reacciones previas a un medio de contraste son tres veces más susceptibles que otros pacientes. Sin embargo, la sensibilidad a los medios de contraste no parece aumentar con los exámenes repetidos. La mayoría de las reacciones adversas a los agentes de contraste intravascular aparecen dentro de uno o tres minutos después del inicio de la inyección, pero pueden ocurrir reacciones retrasadas. Las reacciones retrasadas que generalmente involucran la piel pueden ocurrir de forma rara en 2-3 días (rango de 1 a 7 días) después de la administración de contraste (ver PRECAUCIONES - General ).
Las reacciones alérgicas retrasadas son más frecuentes en pacientes tratados con inmunosimulantes como la interleucina-2.
En addition to the adverse drug reactions reported for iopamidol the following additional adverse reactions have been reported with the use of other intravascular contrast agents y are possible with the use of any water-soluble iodinated contrast agent:
Cardiovascular: hematomas cerebrales petechiae;
Hematológico: neutropenia;
Urogenital: Nefrosis osmótica de células tubulares proximales insuficiencia renal;
Sentidos especiales: Chemosis conjuntival con infección.
Endocrino: hipertiroidismo hipotiroidismo;
Piel y trastornos del tejido subcutáneo: Necrosis de la piel; Las reacciones varían desde leve (por ejemplo, eritema eritema pruritus uticaria y decoloración de la piel) hasta severo: [p. Ej. Síndrome de Stevens-Johnson y necrólisis epidérmica tóxica (SJS/diez) linda pustulosis exantematosa generalizada (AGEP) y reacción farmacológica con eosinofilia y síntomas sistémicos (vestido)].
Interacciones de drogas para isovue-M
Se ha informado toxicidad renal en algunos pacientes con disfunción hepática que recibieron agentes colecistegráficos orales seguidos de agentes de contraste intravascular. Por lo tanto, la administración de agentes intravasculares debe posponerse en cualquier paciente con un trastorno hepático o biliar conocido o sospechoso que recientemente recibió un agente de contraste colecicográfico.
Otras drogas no deben mezclarse con iopamidol.
Advertencias for Isovue-M
Eventos adversos severos La Administración Intratecal LNNNNAdvertida se han informado reacciones adversas graves debido a la administración intratecal inadvertida de medios de contraste yodados que no están indicados para el uso intratecal.
Estas reacciones adversas graves incluyen: convulsiones de muerte de hemorragia cerebral parálisis de coma de coma aracnoiditis aguda insuficiencia renal de paro cardíaco hipertermia y edema cerebral. Se debe prestar especial atención para asegurar que este medicamento no se administre inadvertidamente intratecalmente.
General
Los medios de contraste yodado no iónico inhiben la coagulación de la sangre in vitro menos que los medios de contraste iónico. La coagulación se ha informado cuando la sangre permanece en contacto con jeringas que contienen medios de contraste no iónico.
Se han informado eventos tromboembólicos graves raramente fatales que causan infarto y accidente cerebrovasculares miocárdicos durante los procedimientos angiográficos con medios de contraste iónico y no iónico. Por lo tanto, es necesaria una técnica de administración intravascular meticulosa, particularmente durante los procedimientos angiográficos para minimizar los eventos tromboembólicos. Numerosos factores que incluyen la duración del procedimiento del catéter y la jeringa del estado de enfermedad subyacente y los medicamentos concomitantes pueden contribuir al desarrollo de eventos tromboembólicos. Por estas razones, se recomiendan técnicas angiográficas meticulosas, incluida una atención cercana al uso de la manipulación del cátedra y el catéter de los sistemas múltiples y/o los tálvulas de tres vías, el catéter frecuente con soluciones salinas heparinizadas y minimizando la longitud del procedimiento. Se ha informado que el uso de jeringas de plástico en lugar de las jeringas de vidrio disminuye pero no elimina la probabilidad de in vitro coagulación.
Se debe ejercer precaución en pacientes con función renal gravemente deteriorada aquellos con enfermedad o anuria renal y hepática combinada, particularmente cuando se administran dosis más grandes.
Los agentes de contraste de diagnóstico radiopaco son potencialmente peligrosos en pacientes con mieloma múltiple u otra paraproteinemia, particularmente en aquellos con anuria terapéuticamente resistente. El mieloma ocurre más comúnmente en personas mayores de 40 años. Aunque ni el agente de contraste ni la deshidratación se han demostrado por separado como la causa de la anuria en pacientes mielomatosos, se ha especulado que la combinación de ambos puede ser causal. El riesgo en pacientes mielomatosos no es una contraindicación; Sin embargo, se requieren precauciones especiales.
Los medios de contraste pueden promover la hoza en personas que son homocigotas para la enfermedad de las células falciformes cuando se inyectan por vía intravenosa o intraarterial.
La administración de materiales radiopacos a pacientes conocidos o sospechosos de tener feocromocitoma debe realizarse con extrema precaución. Si en opinión del médico, los posibles beneficios de tales procedimientos superan los riesgos considerados, se pueden realizar los procedimientos; Sin embargo, la cantidad de medio radiopaco inyectado debe mantenerse al mínimo absoluto. La presión arterial debe evaluarse durante todo el procedimiento y las medidas para el tratamiento de una crisis hipertensiva deben estar disponibles. Estos pacientes deben ser monitoreados muy de cerca durante los procedimientos de contraste mejorados.
Los informes de tormenta tiroidea después del uso de agentes de diagnóstico radiopaco yodados en pacientes con hipertiroidismo o con un nódulo tiroideo que funciona de manera autónoma sugiere que este riesgo adicional se evaluará en tales pacientes antes del uso de cualquier medio de contraste.
Disfunción tiroidea en pacientes pediátricos de 0 a 3 años de edad
La disfunción tiroidea caracterizada por hipotiroidismo o supresión transitoria de la tiroides se ha informado después de la exposición única y las exposiciones múltiples a medios de contraste yodados en pacientes pediátricos de 0 a 3 años de edad.
Edad más joven Muy bajo peso al nacer prematuro subyacente a las condiciones médicas que afectan el ingreso de la función tiroidea a las unidades de cuidados intensivos neonatales o pediátricos y las condiciones cardíacas congénitas se asocian con un mayor riesgo de hipotiroidismo después de la exposición a ICM. Los pacientes pediátricos con afecciones cardíacas congénitas pueden tener un mayor riesgo dado que a menudo requieren altas dosis de contraste durante los procedimientos cardíacos invasivos.
Una tiroides poco activa durante la vida temprana puede ser dañino para el desarrollo cognitivo y neurológico y puede requerir una terapia de reemplazo de hormonas tiroideas. Después de la exposición a ICM, individualice el monitoreo de la función tiroidea basada en factores de riesgo subyacentes, especialmente en los neonatos a término y prematuro.
Reacciones adversas cutáneas graves
Las reacciones adversas cutáneas (SCAR) graves pueden desarrollarse de 1 hora a varias semanas después de la administración del agente de contraste intravascular. Estas reacciones incluyen el síndrome de Stevens-Johnson y la necrólisis epidérmica tóxica (SJS/diez) pustulosis exantematosa generalizada (AGEP) y la reacción del fármaco con eosinofilia y síntomas sistémicos (vestimenta). La gravedad de la reacción puede aumentar y el tiempo de inicio puede disminuir con la administración repetida del agente de contraste; Los medicamentos profilácticos no pueden prevenir ni mitigar reacciones adversas cutáneas graves. Evite administrar isovue a pacientes con antecedentes de una reacción adversa cutánea grave a Isovue.
Precauciones for Isovue-M
General
Los procedimientos de diagnóstico que implican el uso de cualquier agente radiopaco deben llevarse a cabo bajo la dirección del personal con el entrenamiento previo y con un conocimiento exhaustivo del procedimiento particular que se realizará. Las instalaciones apropiadas deben estar disponibles para hacer frente a cualquier complicación del procedimiento, así como para el tratamiento de emergencia de la reacción severa al agente de contraste. Después de la administración parenteral de un agente radiopaco, el personal competente y las instalaciones de emergencia deben estar disponibles durante al menos 30 a 60 minutos, ya que pueden ocurrir reacciones retrasadas graves. Se debe tener precaución en pacientes hidratantes con afecciones subyacentes que pueden empeorar por una sobrecarga de fluidos, como insuficiencia cardíaca congestiva .
La deshidratación preparatoria es peligrosa y puede contribuir a insuficiencia renal aguda en pacientes con pacientes diabéticos avanzados de enfermedad vascular y en pacientes no diabéticos susceptibles (a menudo ancianos con enfermedad renal preexistente). Los pacientes deben estar bien hidratados antes y después de la administración de iopamidol.
Siempre se debe considerar la posibilidad de una reacción que incluya reacciones fatales graves que amenazan la vida (ver (ver Reacciones adversas ).
Los pacientes con mayor riesgo incluyen aquellos con antecedentes de una reacción previa a un medio de contraste de pacientes con una sensibilidad conocida al yodo per se y a los pacientes con una hipersensibilidad clínica conocida (fiebre del heno de asma bronquial y alergias alimentarias). La aparición de reacciones idiosincráticas severas ha provocado el uso de varios métodos de prueba previos. Sin embargo, no se puede confiar en la prueba previa para predecir reacciones severas y puede ser peligroso para el paciente. Se sugiere que un historial médico exhaustivo con énfasis en la alergia y la hipersensibilidad antes de la inyección de cualquier medio de contraste puede ser más preciso que la prueba previa para predecir posibles reacciones adversas. Una historia positiva de alergias o hipersensibilidad no contradica arbitrariamente el uso de un agente de contraste donde se cree que un procedimiento diagnóstico es esencial, pero se debe tener precaución. Se debe considerar la premedicación con antihistamínicos o corticosteroides para evitar o minimizar posibles reacciones alérgicas en tales pacientes. Informes recientes indican que dicho pretratamiento no impide reacciones graves que potencialmente mortalvían la vida, pero pueden reducir tanto su incidencia como la gravedad.
Las afecciones preexistentes, como los marcapasos o los medicamentos cardíacos, específicamente los betablockers pueden enmascarar o alterar los signos o síntomas de una reacción anafilactoides, así como enmascarar o alterar la respuesta a medicamentos particulares utilizados para el tratamiento. Por ejemplo, los betabloqueantes inhiben una respuesta taquicardíaca y pueden conducir al diagnóstico incorrecto de una reacción vasovagal en lugar de una reacción anafilactoide. La atención especial a esta posibilidad es particularmente crítica en pacientes que padecen reacciones graves que amenazan la vida.
General anesthesia may be indicated in the performance of some procedures in selected patients; however a higher incidence of adverse reactions has been reported with radiopaque media in anesthetized patients which may be attributable to the inability of the patient to identify untoward symptoms or to the hypotensive effect of anesthesia which can reduce cardiac output y increase the duration of exposure to the contrast agent.
A pesar de que la osmolalidad del iopamidol es baja en comparación con los agentes iónicos basados en diatrizoato o iootalamato de concentración de yodo comparable, el aumento transitorio potencial en la carga osmótica circulatoria en pacientes con insuficiencia cardíaca congestiva requiere precaución durante la inyección. Estos pacientes deben observarse durante varias horas después del procedimiento para detectar trastornos hemodinámicos tardíos. Puede producirse dolor e hinchazón del sitio de inyección. En la mayoría de los casos se debe a la extravasación de medio de contraste. Las reacciones suelen ser transitorias y se recuperan sin secuelas. Sin embargo, la inflamación e incluso la necrosis de la piel se han visto en ocasiones muy raras.
En angiographic procedures the possibility of dislodging plaques or damaging or perforating the vessel wall or inducing vasospasm y or subsequent ischemic events should be borne in mind during catheter manipulations y contrast medium injection. Test injections to ensure proper catheter placement are suggested.
Arteriografía coronaria selectiva Debe realizarse solo en pacientes seleccionados y aquellos en los que los beneficios esperados superan el riesgo de procedimiento. Los riesgos inherentes de angiocardiografía En los pacientes con enfisema pulmonar crónico debe sopesarse en contra de la necesidad de realizar este procedimiento. La angiografía debe evitarse siempre que sea posible en pacientes con homocistinuria debido al riesgo de inducir trombosis y embolia. Ver también Uso pediátrico .
¿Qué tipo de droga es valsartán?
En addition to the general precautions previously described special care is required when venography is performed in patients with suspected thrombosis phlebitis severe ischemic disease local infection or a totally obstructed venous system.
Se necesita extrema precaución durante la inyección de medios de contraste para evitar la extravasación y se recomienda la fluoroscopia. Esto es especialmente importante en pacientes con enfermedad arterial o venosa grave.
Interacciones de prueba de drogas/laboratorio
Los resultados de PBI y estudios de absorción de yodo radiactivo que dependen de las estimaciones de yodo no reflejarán con precisión la función tiroidea durante hasta 16 días después de la administración de medios de contraste yodados. Sin embargo, las pruebas de la función tiroidea no dependen de las estimaciones de yodo, p. La absorción de resina T3 y los ensayos de tiroxina total o libre (T4) no se ven afectados.
Cualquier prueba que pueda verse afectada por los medios de contraste debe realizarse antes de la administración del medio de contraste.
Hallazgos de pruebas de laboratorio
En vitro Los estudios con sangre animal mostraron que muchos agentes de contraste radiopaco, incluido el iopamidol, produjeron una ligera depresión de los factores de coagulación plasmática, incluida PRECAUCIONES General ).
Los cambios transitorio pueden ocurrir en la transaminasa oxaloacética glutámica sérica sérica sérica sérica sérica sérica sérica sérica sérica sérica en suero; Puede ocurrir la albuminuria transitoria.
Estos hallazgos no se han asociado con manifestaciones clínicas.
Carcinogénesis Mutagénesis Deterioro de la fertilidad
No se han realizado estudios a largo plazo en animales para evaluar el potencial cancerígeno. No se obtuvo evidencia de toxicidad genética en in vitro pruebas.
Embarazo
Efectos teratogénicos
Los estudios de reproducción se han realizado en ratas y conejos a dosis de hasta 2.7 y 1.4 veces la dosis humana máxima recomendada (1.48 gi/kg en un individuo de 50 kg) respectivamente y no han revelado evidencia de fertilidad o daño alterado al feto debido al iopamidol. Sin embargo, no hay estudios adecuados y bien controlados en mujeres embarazadas. Debido a que los estudios de reproducción animal no siempre predicen la respuesta humana, este medicamento debe usarse durante el embarazo solo si claramente se necesita.
Madres lactantes
No se sabe si este medicamento se excreta en la leche humana. Debido a que muchas drogas se excretan en la leche humana, se debe ejercer la precaución cuando el iopamidol se administra a una mujer lactante.
Uso pediátrico
La seguridad y la efectividad en los niños se han establecido en angiocardiografía pediátrica y tomografía computarizada (cabeza y cuerpo). Los pacientes pediátricos con mayor riesgo de experimentar eventos adversos durante la administración de medio de contraste pueden incluir a aquellos que tienen asma una sensibilidad a los medicamentos y/o alérgenos, enfermedad cardíaca cianótica, insuficiencia cardíaca congestiva, una creatinina sérica mayor de 1,5 mg/dL o aquellos menores de 12 meses de edad.
Las pruebas de función tiroidea indicativas de disfunción tiroidea caracterizada por hipotiroidismo o supresión transitoria de tiroides se han informado de manera poco común después de la administración de medios de contraste yodado en pacientes pediátricos, incluidos los recién nacidos a término y prematuro; Algunos pacientes fueron tratados por hipotiroidismo. Después de la exposición a los medios de contraste yodados, individualizar el monitoreo de la función de la tiroides en pacientes pediátricos de 0 a 3 años de edad en función de los factores de riesgo subyacentes, especialmente en los neonatos a plazo y prematuro (ver Advertencias y Reacciones adversas ).
Información de sobredosis para isovue-M
El tratamiento de una sobredosis de un medio de contraste radiopaco inyectable está dirigido hacia el apoyo de todas las funciones vitales y la institución rápida de la terapia sintomática.
Contraindicaciones para isovue-m
Ninguno.
Farmacología clínica for Isovue-M
Entravascular injection of a radiopaque diagnostic agent opacifies those vessels in the path of flow of the contrast medium permitting radiographic visualization of the internal structures of the human body until significant hemodilution occurs.
Después de la inyección intravascular, los agentes de diagnóstico radiopaco se diluyen inmediatamente en el plasma circulante. Los cálculos del volumen aparente de distribución en estado estacionario indican que el iopamidol se distribuye entre el volumen sanguíneo circulante y otro líquido extracelular; Parece que no hay una deposición significativa de iopamidol en los tejidos. La distribución uniforme de iopamidol en el fluido extracelular se refleja en su utilidad demostrada en imágenes tomográficas calculadas de la cabeza y el cuerpo después de la administración intravenosa.
La farmacocinética del iopamidol administrado por vía intravenosa en sujetos normales se ajusta a un modelo abierto de dos compartimentos con eliminación de primer orden (una fase alfa rápida para la distribución de fármacos y una fase beta lenta para la eliminación del fármaco). El suero de eliminación o la vida media plasmática es de aproximadamente dos horas; La vida media no depende de la dosis. No se produce una desiodinación o biotransformación de metabolismo significativo.
Iopamidol is excreted mainly through the kidneys following intravascular administration. En patients with impaired renal function the elimination half-life is prolonged dependent upon the degree of impairment. En the absence of renal dysfunction the cumulative urinary excretion for iopamidol expressed as a percentage of administered intravenous dose is approximately 35 to 40 percent at 60 minutes 80 to 90 percent at 8 hours y 90 percent or more in the 72- to 96-hour period after administration. En normal subjects approximately one percent or less of the administered dose appears in cumulative 72- to 96-hour fecal specimens.
Isovue se puede visualizar en el parénquima renal en 30-60 segundos después de la rápida administración intravenosa. La opacificación de los cálices y las pelvas en pacientes con función renal normal se hace evidente en 1 a 3 minutos con un contraste óptimo que ocurre entre 5 y 15 minutos. En pacientes con deterioro renal, la visualización de contraste puede retrasarse.
Iopamidol displays little tendency to bind to serum or plasma proteins. No evidence of en vano La activación del complemento se ha encontrado en sujetos normales. Los estudios en animales indican que el iopamidol no cruza la barrera hematoencefálica en ningún grado significativo después de la administración intravascular.
Isovue (inyección de iopamidol) mejora las imágenes del cerebro tomográfico computarizado a través del aumento de la eficiencia radiográfica. El grado de mejora de la visualización de la densidad del tejido está directamente relacionado con el contenido de yodo en una dosis administrada; Los niveles pico de sangre de yodo ocurren inmediatamente después de la inyección rápida de la dosis. Estos niveles caen rápidamente en cinco a diez minutos. Esto puede explicarse por la dilución en los compartimentos de fluido vascular y extracelular que provoca una caída aguda inicial en la concentración plasmática. El equilibrio con los compartimentos extracelulares se alcanza en aproximadamente diez minutos a partir de entonces, la caída se vuelve exponencial. La mejora máxima del contraste se produce con frecuencia después de alcanzar los niveles máximos de yodo en sangre. El retraso en la mejora máxima del contraste puede variar de cinco a cuarenta minutos, dependiendo de los niveles máximos de yodo alcanzado y el tipo de célula de la lesión. Este retraso sugiere que la mejora de contraste radiográfico depende al menos en parte de la acumulación de yodo dentro de la lesión y fuera del grupo de sangre, aunque el mecanismo por el cual esto ocurre no está claro. La mejora radiográfica de las lesiones no tumorales, como las malformaciones arteriovenosas y los aneurismas, probablemente depende del contenido de yodo del grupo de sangre circulante.
En CT head imaging ISOVUE (Iopamidol Enjection) does not accumulate in normal brain tissue due to the presence of the blood-brain barrier. The increase in x-ray absorption in normal brain is due to the presence of contrast agent within the blood pool. A break in the blood-brain barrier such as occurs in malignant tumors of the brain allows the accumulation of the contrast medium within the interstitial tissue of the tumor. Adjacent normal brain tissue does not contain the contrast medium.
En nonneural tissues (during computed tomography of the body) iopamidol diffuses rapidly from the vascular into the extravascular space. Encrease in x-ray absorption is related to blood flow concentration of the contrast medium y extraction of the contrast medium by interstitial tissue of tumors since no barrier exists. Contrast enhancement is thus due to the relative differences in extravascular diffusion between normal y abnormal tissue quite different from that in the brain.
Se ha demostrado que la farmacocinética del iopamidol en el tejido normal y anormal es variable. La mejora del contraste parece ser mayor poco después de la administración del medio de contraste y después de la administración intraarterial en lugar de intravenosa. Por lo tanto, la mayor mejora se puede detectar mediante una serie de escaneos consecutivos de dos a tres segundos realizados justo después de la inyección (dentro de 30 a 90 segundos), es decir, imágenes tomográficas calculadas dinámicas.
Información del paciente para isovue-M
Los pacientes que reciben agentes de diagnóstico radiopaco inyectables deben recibir instrucciones de:
- Enform your physician if you are pregnant.
- Enform your physician if you are diabetic or if you have multiple myeloma pheochromocytoma homozygous sickle cell disease or known thyroid disorder (see Advertencias ).
- Enform your physician if you are allergic to any drugs food or if you had any reactions to previous injections of substances used for x-ray procedures (see PRECAUCIONES - General ).
- Enform your physician about any other medications you are currently taking including nonprescription drugs before you have this procedure.
- Aconseje a los pacientes que informen a su médico si desarrollan una erupción después de recibir isovue.
- Asesorar a los padres/cuidadores sobre el riesgo de desarrollar disfunción tiroidea después de la administración de isovue. Asesorar a los padres/cuidadores sobre cuándo buscar atención médica para su hijo para monitorear la función tiroidea (ver Advertencias ).